
Thomas Dalton
0
5258
1162
Wissenschaftler könnten endlich den mysteriösen Übergang hinter einem jahrhundertealten Chemieexperiment verstehen. Die Details dieser Umwandlung, bei der die Zugabe von Elektronen zu einer hellblauen Ammoniaklösung diese in eine glänzende metallische Bronze verwandelt, sind Wissenschaftlern lange entgangen.
Die neue Studie enthüllt die subtilen Details dieser Änderung und zeigt, dass diese Transformation eher allmählich als plötzlich erfolgt. "Was wir erfolgreich gemacht haben, ist, dass wir ziemlich genau verstanden haben, wie sich diese Lösungen in einem breiten Konzentrationsbereich mithilfe einer Mikrojet-Technik verhalten", sagte der Co-Autor der Studie, Ryan McMullen, ein Doktorand in Chemie an der University of Southern California . Diese Technik, bei der haardünne Ströme der Lösung durch ein Vakuum geschossen werden, wurde bisher noch nicht bei der glänzenden Flüssigkeit angewendet.
Und die Entdeckung könnte in Zukunft neue Arten von Reaktionen in der organischen Chemie eröffnen, sagte McMullen .
Verbunden: 8 chemische Elemente, von denen Sie noch nie gehört haben
Was ist ein Metall??
Metalle sind eine vielfältige Gruppe. Einige wie Lithium sind leicht genug, um zu schweben, während andere wie Blei oder Osmium extrem dicht sind. Einige erfordern unglaublich hohe Temperaturen, um zu schmelzen, während andere leicht schmelzen (Quecksilber schmilzt beispielsweise bei minus 38,3 Grad Celsius oder minus 37,9 Grad Fahrenheit). Gemeinsam ist den Metallen letztendlich ihre Fähigkeit, Elektrizität am absoluten Nullpunkt zu leiten, dem Punkt, an dem die molekulare Bewegung durch Wärme im Wesentlichen anhält.
Aber wie wandeln sich einige Nichtmetalle in Metalle um? In einer neuen Studie beantworteten die Forscher diese Frage, indem sie flüssigem Ammoniak Metalle hinzufügten.
Zunächst kondensierten die Forscher Ammoniak, ein bei Raumtemperatur ein Gas, zu einer Flüssigkeit, indem sie es auf minus 33 ° F abkühlten. Sie fügten dann entweder Natrium, Lithium oder Kalium hinzu, die alle Alkalimetalle sind. (Bekanntlich reagieren diese Metalle explosionsartig, wenn sie in Wasser getaucht werden.) Die Experimente wurden in Zusammenarbeit mit Wissenschaftlern der Tschechischen Akademie der Wissenschaften und des Fritz-Haber-Instituts der Max-Planck-Gesellschaft in Berlin sowie Forschern in Japan und Frankreich durchgeführt.
Verbunden: Die Top 10 der größten Explosionen aller Zeiten
Das Ergebnis war eine erwartete Reaktion: Das flüssige Ammoniak zog Elektronen aus dem Metall. Diese Elektronen wurden dann zwischen den Ammoniakmolekülen eingeschlossen und erzeugten die sogenannten solvatisierten Elektronen, die die Forscher untersuchen wollten. Bei niedrigen Konzentrationen war das Ergebnis eine blaue, nichtmetallische Flüssigkeit. Als sich die solvatisierten oder eingefangenen Elektronen häuften, ging die Lösung in glänzende Bronze über.
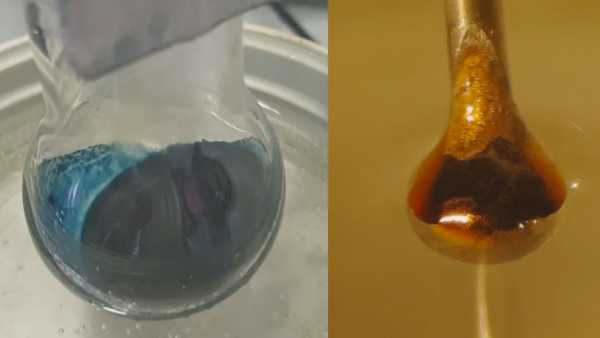
Die nächste Herausforderung bestand darin zu untersuchen, wie sich die solvatisierten Elektronen bei unterschiedlichen Konzentrationen verhalten. Dies beinhaltete das Schießen eines Mikrostrahls der Lösung - ungefähr so breit wie ein menschliches Haar - durch einen Strahl von Synchrotron-Röntgenstrahlen, bei denen es sich um hochenergetische Röntgenstrahlen handelt. Die Röntgenstrahlen erregten die solvatisierten Elektronen und ließen sie aus ihrem Flüssigkeitskäfig aus Ammoniakmolekülen springen. Die Forscher konnten dann messen, wie viel Energie benötigt wurde, um die solvatisierten Elektronen freizusetzen.
Die Forscher fanden heraus, dass das Muster der Energiefreisetzung umso besser mit dem übereinstimmt, was in einem Metall zu sehen ist, je höher die Konzentration der solvatisierten Elektronen ist. Das bedeutet Folgendes: Wenn Sie die Energiemenge grafisch darstellen, die erforderlich ist, um Elektronen aus ihrem flüssigen Ammoniakkäfig freizusetzen, haben Metalle normalerweise eine sogenannte "Fermi-Kante", einen sehr abrupten Übergang, sagte McMullen. Bei niedrigeren Konzentrationen solvatisierter Elektronen ähnelt dieser Energiefreisetzungsgraph eher einem abgerundeten Hügel. Erst bei höheren Elektronenkonzentrationen trat diese Fermi-Kante auf. Die Kante spiegelt wider, wie viel Energie Elektronen bei einer bestimmten Temperatur haben, fügte McMullen hinzu.
"Wenn Sie die Konzentration auf den Metallbereich erhöhen, entsteht dieses wunderbare Muster, das für ein Metall sehr, sehr charakteristisch ist", sagte McMullen.
Die Ergebnisse waren interessant, weil sie zeigten, dass die metallähnliche Flüssigkeit, die durch die Kombination von Alkalimetallen und Ammoniak entsteht, tatsächlich ein Metall auf einer fundamentalen physikalischen Ebene ist, sagte er.
"Es ist ein echtes Metall, es sieht nicht nur so aus", sagte McMullen.
Solvatisierte Elektronen mit niedrigerer Konzentration werden in einer Art Reaktion verwendet, die als Birkenreaktion bezeichnet wird und Elektronen zu molekularen Strukturen hinzufügt, die als aromatische Ringe bezeichnet werden. Diese Art von Reaktion wurde bei der Herstellung der ersten oralen Verhütungspillen in den 1950er Jahren verwendet, sagte McMullen. Durch das Verständnis, wie solvatisierte Elektronen in hohen Konzentrationen funktionieren, können Forscher möglicherweise neue Arten chemischer Reaktionen finden, sagte er. Zum Beispiel könnten sie die solvatisierten Elektronen mit Lichtstrahlen anregen, um sie dazu zu bringen, sich auf neue Weise zu verhalten.
"Wenn Sie die Elektronen ein wenig kitzeln, damit sie energetisch angeregt werden, können Sie einige verrückte Reaktionen untersuchen, die sonst niemals auftreten würden", sagte McMullen.
Die Forscher berichteten über ihre Ergebnisse am 5. Juni in der Zeitschrift Science.
Alle Kommentare anzeigen (2)














